Нитрид титана
Нитрид титана — бинарное химическое соединение титана с азотом.
Представляет собой фазу внедрения с широкой областью гомогенности, которая составляет от 14,8 до 22,6 % азота (по массе), что можно обозначить брутто-формулами от Ti10N6 до TiN соответственно.
Физические свойства
Нитрид титана представляет собой порошок жёлто-коричневого цвета, а в компактном состоянии приобретает золотистую окраску.
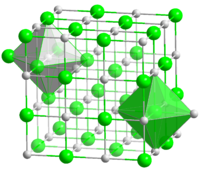
Имеет кубическую гранецентрированную решётку типа NaCl, пространственная группа Fm3m, с периодом а = 0,4235 нм.
- Удельное электрическое сопротивление 40 мкОм∙см.
- Коэффициент линейного теплового расширения 9,35∙10−6 1/K (25-1100 °C)
- Микротвердость 2050 кгc/мм2 .
- Модуль упругости 25600 кг/мм2.
Получение
Нитрид титана можно получить одним из следующих способов.
- Непосредственным насыщением титана азотом:
- Взаимодействием тетрахлорида титана со смесью азота и водорода:
- Разложением аминохлоридов титана:
- Восстановлением оксида титана углеродом в среде азота:
- Синтезом в плазме:
- Самораспространяющимся высокотемпературным синтезом:
Химические свойства
Нитрид титана устойчив к окислению на воздухе до 700—800 °C, при этих же температурах сгорает в токе кислорода:
2 TiN + 2 O 2 ⟶ 2 TiO 2 + N 2 {displaystyle {ce {2TiN + 2O2 -> 2TiO2 + N2}}} .При нагреве до 1200 °C в среде водорода или в смеси азота и водорода нитрид титана инертен.
Нитрид титана стехиометрического состава проявляет стойкость к CO, но медленно реагирует с CO2 по реакции:
2 TiN + 4 CO 2 ⟶ 2 TiO 2 + 4 CO + N 2 {displaystyle {ce {2TiN + 4CO2 -> 2TiO2 + 4CO + N2}}} .Реагирует на холоде с фтором:
2 TiN + 4 F 2 ⟶ 2 TiF 4 + N 2 {displaystyle {ce {2TiN + 4F2 -> 2TiF4 + N2}}} .Хлор не взаимодействует с нитридом титана до 270 °C, но реагирует с ним при температурах свыше 300—400 °C:
2 TiN + 4 Cl 2 ⟶ 2 TiCl 4 + N 2 {displaystyle {ce {2TiN + 4Cl2 -> 2TiCl4 + N2}}} .При температуре 1300 °C хлороводород взаимодействует с TiN {displaystyle {ce {TiN}}} с образованием газообразных хлоридов титана и азота с водородом.
Взаимодействует с дицианом образуя карбонитрид титана:
10 TiN + ( CN ) 2 ⟶ 2 Ti 5 N 4 C + 2 N 2 {displaystyle {ce {10TiN + (CN)2 -> 2Ti5N4C + 2N2}}} .При комнатной температуре, по отношению к серной, соляной, фосфорной, хлорной кислотам, а также к смесям хлорной и соляной, щавелевой и серной кислот, нитрид титана является стойким соединением. Кипящие кислоты (соляная, серная и хлорная) слабо взаимодействуют с TiN {displaystyle {ce {TiN}}} . На холоде малоустойчив против растворов гидроксида натрия. Взаимодействует с азотной кислотой, а в присутствии сильных окислителей растворяется плавиковой кислотой.
Нитрид титана является стойким к действию расплавов олова, висмута, свинца, кадмия и цинка. При высокой температуре разрушается оксидами железа (Fe2O3), марганца (MnO), кремния (SiO2) и стеклом.
Применение
Применяется как жаропрочный материал, в частности из него делают тигли для плавки металлов в бескислородной атмосфере.
В металлургии это соединение встречается в виде относительно крупных (единицы и десятки микрон) неметаллических включений в сталях, легированных титаном. Такие включения имеют на шлифах, как правило, форму квадратов и прямоугольников, их легко идентифицировать методом металлографического анализа. Такие крупные частицы нитрида титана, образующиеся из расплава, приводят к ухудшению качества литого металла.
Нитрид титана используется для создания износостойких покрытий металлорежущего инструмента, также для зубных протезов жёлтого «под золото» цвета.
Используется в микроэлектронике в качестве диффузионного барьера совместно с медной металлизацией и др.
Также нитрид титана применяется в качестве износостойкого и декоративного покрытия. Изделия, покрытые им, по внешнему виду похожи на золото и могут иметь различные оттенки, в зависимости от соотношения металла и азота в соединении. Нанесение покрытия из нитрида титана производится в специальных камерах термодиффузионным методом. При высокой температуре титан и азот реагируют вблизи поверхности покрываемого изделия и диффундируют в саму структуру металла.
Соединение не используется для покрытия электрических контактов.